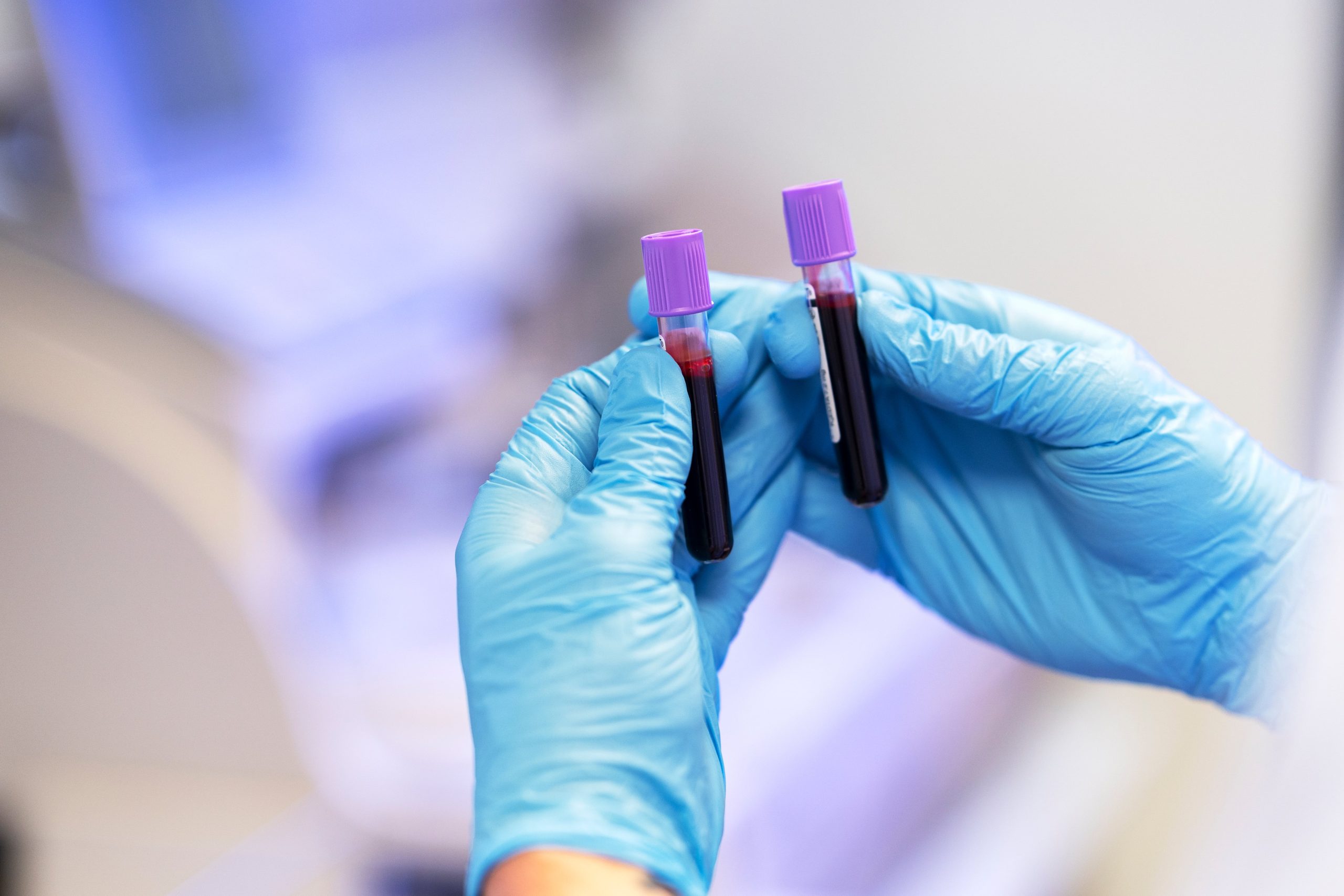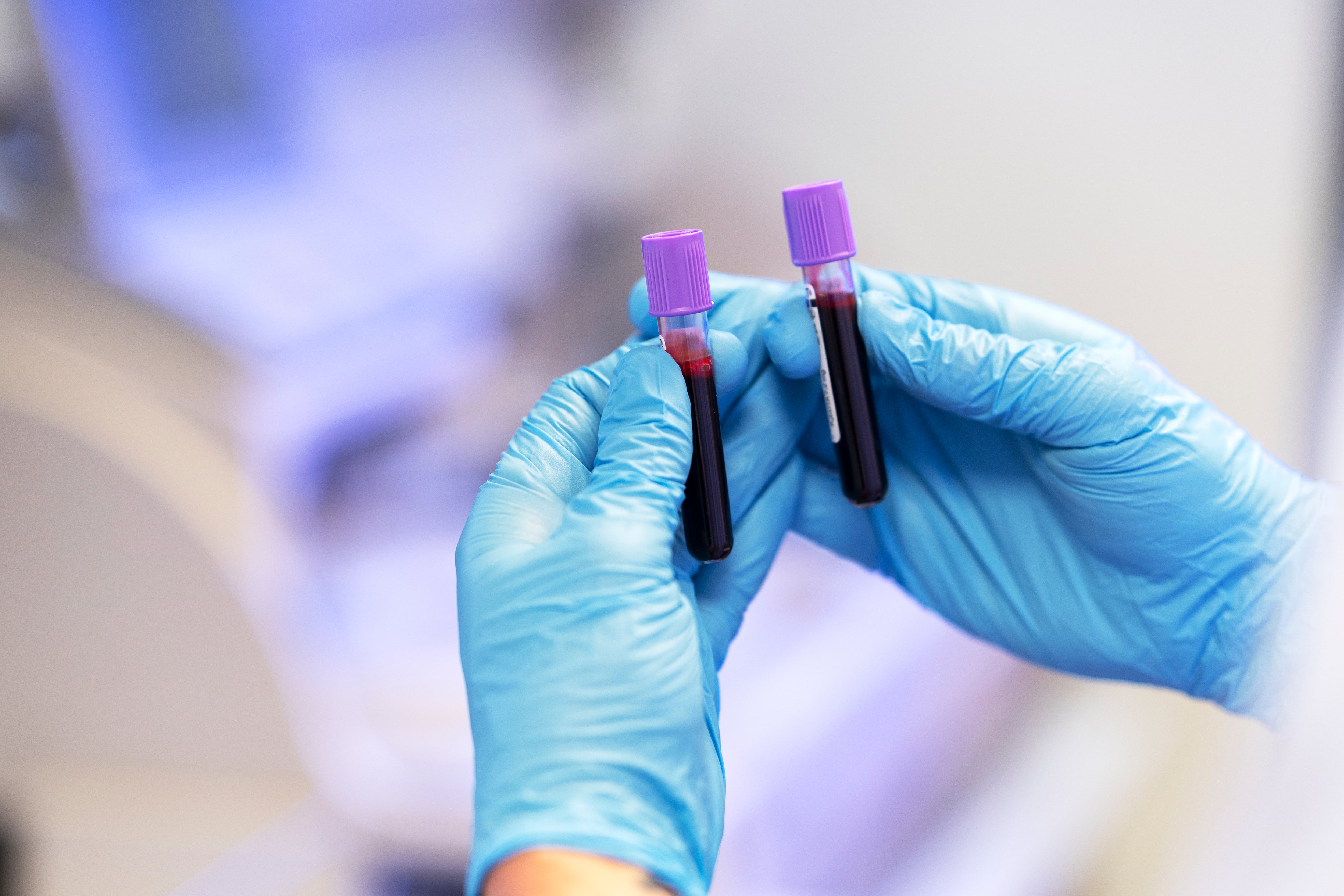
Cada año, miles de personas mueren por hemorragias internas que no se pueden frenar con presión manual ni con los hemostáticos disponibles en cirugía de urgencia.
Son sangrados en órganos como el hígado o el bazo, donde el tiempo entre la herida y el coágulo puede ser la diferencia entre vivir y morir.
Investigadores de la Universidad McGill, en Montreal, Canadá, lograron producir coágulos de sangre artificiales que se forman en menos de cinco segundos, resisten trece veces más que los naturales y aceleran la regeneración del tejido dañado.
La investigación se publicó en la revista Nature.
El estudio fue liderado por Shuaibing Jiang y Jianyu Li, del Departamento de Ingeniería Mecánica de la Universidad McGill.
El equipo incluyó investigadores de la Universidad de Colorado Boulder, Estados Unidos, y la Universidad de Columbia Británica, el Instituto de Investigación de Sangre Versiti y la Universidad de Toronto, en Canadá.
Por qué los coágulos naturales fallan

Los glóbulos rojos ocupan cerca del 45% del volumen total de la sangre, pero dentro de un coágulo natural no aportan resistencia mecánica.
La proteína que le da estructura, la fibrina, una red de hilos que atrapa las células, representa menos del 1% del volumen total.
Con tan poco material estructural, el coágulo se fractura con facilidad y puede desprenderse de la herida antes de que el tejido sane.
Además, el proceso de coagulación natural puede tardar varios minutos, lo que en una hemorragia grave resulta fatal.
El objetivo de los investigadores fue convertir a los glóbulos rojos en piezas estructurales del coágulo, sin interferir con la coagulación natural y sin dañar las células. Buscaron que la estrategia acelerara la formación del coágulo y le diera resistencia real ante la presión de una hemorragia activa.
Pegar células como piezas de un rompecabezas

Los investigadores desarrollaron una técnica llamada “coagulación por clic”, que une los glóbulos rojos entre sí mediante química bioortogonal: reacciones químicas que ocurren cerca de sistemas biológicos sin interferir con ellos.
Modificaron la superficie de los glóbulos rojos con un compuesto llamado TCO (trans-cicloocteno), que actúa como un gancho molecular, y prepararon ácido hialurónico con tetrazina (TZ), que funciona como el cierre de ese gancho. Al mezclar ambos componentes, la reacción ocurre en menos de cinco segundos.
El resultado es lo que los investigadores denominaron un “citogel”: una red sólida donde los propios glóbulos rojos son las unidades estructurales.
El estudio señaló que los EBC “se forman en segundos y exhiben un aumento de 13 veces en la tenacidad a la fractura, y una mejora de 4 veces en la energía de adhesión en comparación con los coágulos nativos”.
Los investigadores realizaron pruebas de tracción cíclica, al estirar y soltar el material repetidamente, y midieron la hemoglobina liberada en cada ciclo.

La hemoglobina es la proteína dentro del glóbulo rojo que transporta oxígeno; su liberación indica que la célula se rompió.
Cuanto más se estiraba el citogel, más hemoglobina se detectaba, lo que confirmó que la ruptura de los glóbulos rojos es el mecanismo de resistencia: al romperse, disipan energía y evitan que la fractura se propague.
En ratas con heridas profundas en el hígado, la pérdida de sangre bajó de 1.813 a 24 miligramos, y el tiempo hasta detener el sangrado cayó de 265 segundos a solo 5 segundos. El hemostático comercial de referencia tardó 91 segundos y dejó una pérdida de 148 miligramos.
Los hígados tratados con EBC alcanzaron una tasa de recuperación del 100% a los 28 días, frente al 84% del grupo tratado con el producto comercial.
Las adherencias postoperatorias, el tejido cicatricial que une órganos que no deberían estar pegados, se redujeron al 17%, contra el 83% en el otro grupo.
Un material que el cuerpo tolera

Las pruebas de biocompatibilidad mostraron que los EBC no destruyen glóbulos rojos, no activan plaquetas ni células del sistema inmune, y se degradan por completo en ocho semanas. El hígado y los riñones son las vías principales de eliminación, sin evidencia de toxicidad sistémica.
La investigación validó tanto los EBC autólogos, que son preparados con la propia sangre del paciente, como los alogénicos (con sangre de donante compatible en grupo sanguíneo). Los autólogos se preparan en 30 minutos y los alogénicos en aproximadamente diez.

Los experimentos se realizaron en ratas y aún no hay datos en humanos. El estudio indicó que “estudios futuros deben validar el desempeño en escenarios clínicos específicos, particularmente en coagulopatías y otros trastornos de la sangre”.
Para sangrados en arterias de gran calibre, los EBC necesitarían refuerzo mecánico adicional, como mallas o soportes rígidos.
Los investigadores también señalaron la necesidad de desarrollar “modelos mecánicos predictivos que vinculen la arquitectura del citogel y la ruptura celular con las respuestas mecánicas macroscópicas”.