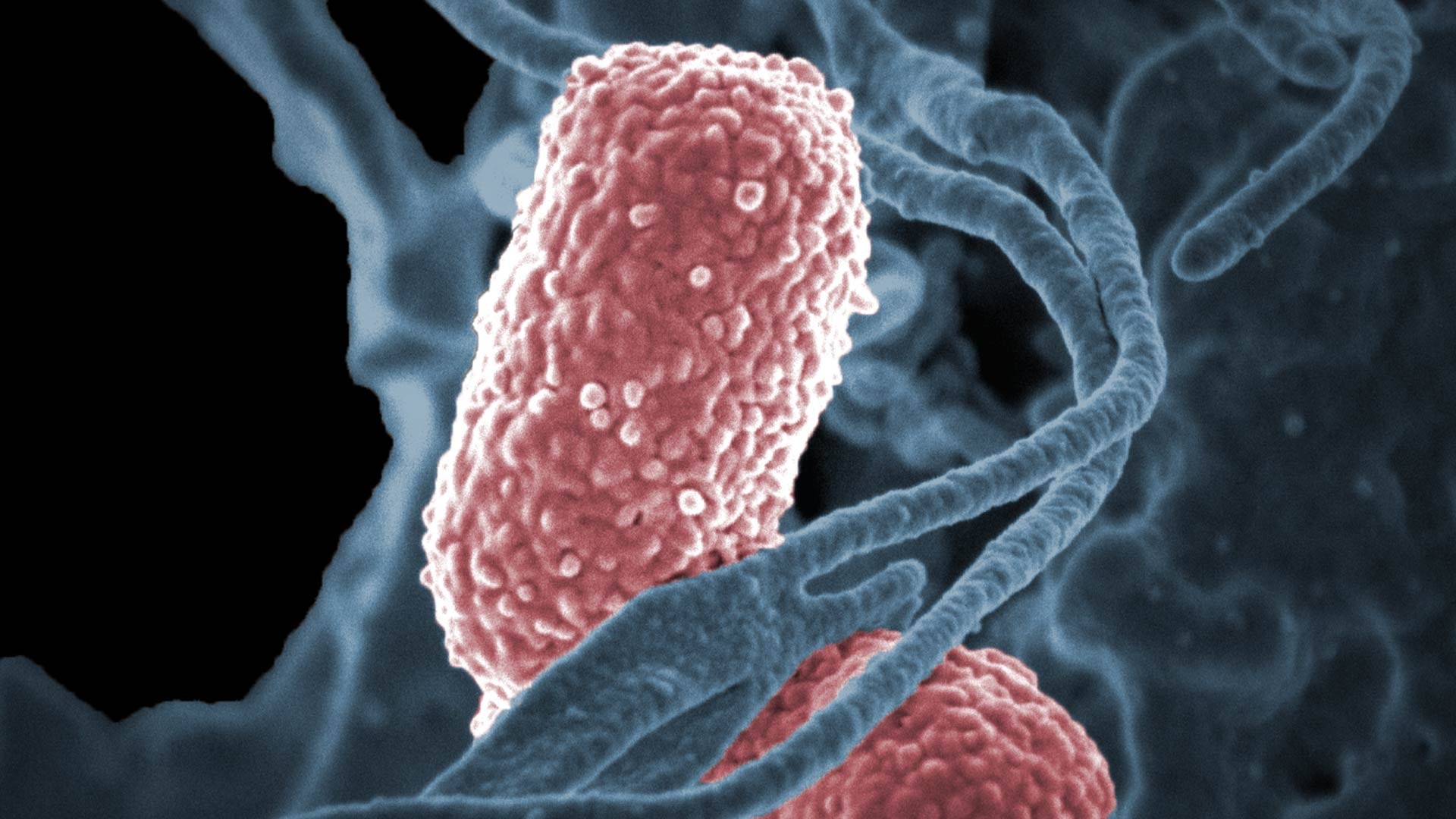
Los estudiosos en microbiología indican que la bacteria de Klebsiella pneumoniae es una de las más peligrosas que existen por su resistencia a diversos tratamientos con antibióticos, por eso se la llama comúnmente superbacteria.
Esa superbacteria es una de las halladas en muestras del producto contaminado Fentanilo HLB Pharma, que causó hasta ahora la muerte 68 pacientes y suma otras víctimas hospitalizadas en diversos centros de salud del país.
Entre las víctimas en estado delicado se encuentra un bebé de 3 meses que permanece internado en terapia intensiva en la clínica Vélez Sarsfield de la ciudad de Córdoba, y pelea por su vida.
Según el estudio microbiológico llevado adelante por los servicios de Bacteriología Especial y Antimicrobianos del Instituto Malbrán, se identificaron cepas de Klebsiella pneumoniae y Klebsiella variicola, ambas con un tipo de resistencia conocida como NDM-5, una carbapenemasa que vuelve ineficaces a la mayoría de los antibióticos.
A esa lista se sumó también Ralstonia pickettii, otro microorganismo con capacidad para provocar infecciones severas en pacientes con sistemas inmunológicos comprometidos.
Cómo actúa la peligrosa bacteria Klebsiella pneumoniae

Klebsiella pneumoniae no es una desconocida para la medicina.
Se trata de una bacteria gramnegativa, encapsulada e inmóvil que habita de forma natural en el tracto gastrointestinal de las personas. En condiciones normales, forma parte de la flora intestinal y cumple funciones beneficiosas, como la digestión o la competencia con otros gérmenes potencialmente más peligrosos. Sin embargo, cuando abandona el intestino y accede a otras áreas del cuerpo, puede provocar infecciones graves.
“Esta bacteria es un problema de salud pública, ya que se ha hecho resistente y cuesta mucho realmente combatirla. Hay veces que salen antibióticos que son de un amplio espectro muy eficaces, pero el mal uso evidentemente le hacen perder su eficacia. Cada día es más resistente a los antibióticos y la mayoría de las veces hay que hacer un cóctel de uno, de dos o de tres antibióticos como para poder dominarla”, explicó a Infobae el infectólogo Hugo Pizzi.
“El patógeno puede atacar cualquier órgano y derivar en una patología peligrosa para el organismo. Puede agredir pulmones, vejiga, riñones, o donde contamine. Generalmente ocasiona cuadros graves y es difícil hallar el tratamiento que la combata eficazmente. Puede dar cualquier tipo de patología, cualquier órgano, desde una meningitis a una miocarditis o neumonía. También influye en el paciente que se contagia. No es lo mismo un organismo sano, equilibrado, bien alimentado, que un diabético, un inmunocomprometido o que está frágil”, agregó el experto.

Según Pizzi, es común hallar esta bacteria como infección intrahospitalaria porque ha quedado dentro de la sala de operaciones o en la contaminación de manos, o en el grifo del quirófano. “Por eso en cada hospital siempre hay un comité de infecciones intrahospitalarias que está haciendo controles y cultivos de determinados lugares constantemente para combatirla”, concluyó.
“Es un microorganismo que puede producir infecciones de pulmón, de intestino, en las vías urinarias o en heridas. Su variedad más conocida y de mayor relevancia clínica es la Klebsiella pneumoniae y en su mayoría se contagia en hospitales, llegando a causar enfermedades graves o incluso la muerte”, explican desde los Institutos de Salud de los Estados Unidos (NIH).
Klebsiella pneumoniae es muy resistente a los antibióticos
El problema de fondo con esta bacteria radica en su creciente resistencia a los antibióticos. Esa capacidad se volvió más agresiva en ambientes hospitalarios donde el uso de fármacos es frecuente, lo que le confirió la categoría de “superbacteria”.
Según el NIH, “esa bacteria resulta peligrosa fuera del intestino. Si llega a otras partes del organismo humano, puede causar infecciones. Normalmente, provocan neumonía, sepsis, infecciones en heridas y en el tracto urinario. Si no se pueden controlar, esas infecciones pueden causar la muerte del enfermo. Uno de los principales problemas que genera esta bacteria es la dificultad de su tratamiento, ya que es resistente a la mayor parte de los antibióticos”.
La historia clínica de Klebsiella pneumoniae es tan antigua como preocupante.
En 1882, el patólogo alemán Carl Friedlander la describió por primera vez al aislarla de pulmones humanos afectados por neumonía. En sus inicios, se la conoció como el bacilo de Friedlander.
Solo cuatro años después, en 1886, recibió su nombre actual. Desde entonces, se convirtió en objeto de estudio en microbiología por su capacidad para colonizar mucosas humanas y por su fuerte asociación con la neumonía, especialmente en personas con enfermedades como diabetes o trastornos por consumo de alcohol.
“Los estudios fenotípicos, moleculares y genómicos de los aislamientos derivados al LNR, procedentes de muestras del producto Fentanilo HLB Pharma y de muestras de hemocultivos de pacientes, permitieron identificar clones únicos relacionados al brote de: Klebsiella pneumoniae (Kpn) metalobetalactamasa (MBL) – no productora de betalactamasa de espectro extendido (BLEE) secuenciotipo 307 y de Ralstonia mannitolilytica. Adicionalmente, a partir de aislamientos provenientes del producto Fentanilo HLB Pharma y de un paciente, se detectó Klebsiella variicola (Kva) productora de metalo-betalactamasa (MBL) NDM-5 y betalactamasa de espectro extendido (BLEE) CTXM-15, de secuenciotipo 971”, publicó el Ministerio de Salud de la Nación a través del último Boletín Epidemiológico Nacional (BEN).

Y completó: “Klebsiella pneumoniae metalobetalactamasa (MBL) no BLEE (betalactamasa de espectro extendido, o sea que no produce las betalactamasas que hidrolizan antibióticos de espectro extendido, como las cefalosporinas) es un patógeno multirresistente de alta relevancia clínica. La especie Klebsiella variicola forma parte del Complejo Klebsiella pneumoniae (CKP), y su diferenciación con otras especies de este Complejo no es posible mediante los sistemas automatizados.”
Hoy es uno de los patógenos más presentes en hospitales.
En Estados Unidos, representa entre el 3 % y el 8 % de las infecciones bacterianas nosocomiales. En Argentina, los últimos hallazgos del Malbrán la ubican en el centro de una investigación de alcance nacional.
No se trata de una sola variedad. Las cepas más resistentes son aquellas que desarrollaron mecanismos como las metalo-beta-lactamasas (MBL), que rompen el anillo betalactámico de muchos antibióticos e impiden su acción.
Entre ellas, se encuentra la cepa NDM-5, identificada en las muestras del fentanilo contaminado. Esta variedad representa un riesgo crítico porque incluso los antibióticos de última línea, como los carbapenémicos, pierden efectividad.
No es la única. Ralstonia pickettii, otra bacteria detectada por el Malbrán, también puede generar infecciones intrahospitalarias, especialmente cuando contamina soluciones que se administran por vía intravenosa. Aunque históricamente se la consideró de baja virulencia, en los últimos años su presencia fue documentada en casos de meningitis, artritis séptica y sepsis. Se trata de un bacilo ambiental, conocido por su capacidad para colonizar entornos estériles, como quirófanos o sistemas de infusión, y su importancia clínica aumentó a la par de su resistencia a los tratamientos disponibles.

Las infecciones por Klebsiella y Ralstonia no suelen transmitirse por el aire.
En cambio, requieren contacto con superficies contaminadas, piel, mucosas, catéteres, ventilación asistida, orina o heridas abiertas. Es por eso que afectan con más frecuencia a pacientes vulnerables, como quienes están en terapia intensiva, neonatos, diabéticos o personas con defensas debilitadas.
En muchos casos, las personas pueden portar la bacteria sin que esta provoque síntomas. Es lo que se conoce como portación asintomática, un estado que aumenta el riesgo de contagio en ambientes hospitalarios. Para estos pacientes, un tratamiento temprano puede ser la diferencia entre una recuperación sin complicaciones o una infección que derive en neumonía, sepsis o la muerte.
El tratamiento actual contra Klebsiella resistente implica una combinación costosa de antibióticos administrados por vía intravenosa. Sin embargo, su eficacia no siempre está garantizada. La Organización Mundial de la Salud ya incluyó a esta bacteria entre las de mayor prioridad para el desarrollo de nuevos antibióticos, dado su impacto sobre la salud pública y su potencial para originar brotes intrahospitalarios.
En 2023, el Centro para el Control y Prevención de Enfermedades (CDC) reportó más de 9.000 casos de infecciones por enterobacterias resistentes a carbapenémicos en Estados Unidos. De ese total, el 80 % correspondía a Klebsiella pneumoniae. Las razones de esta resistencia incluyen mutaciones genéticas, alteraciones en la membrana celular y la producción excesiva de enzimas que destruyen los fármacos.

Según los registros del expediente judicial abierto por la contaminación masiva en Argentina, el 4 de enero fue ordenado el retiro del lote 31.202 de Fentanilo, pero la partida siguió circulando.
El Hospital Italiano de La Plata compró ese mismo lote el 4 de marzo, y lo utilizó incluso después de esa fecha. En total, se produjeron 154.530 ampollas, de las cuales al menos 90.000 continúan sin recuperar.
La situación llevó a la ANMAT a presentar una denuncia penal contra HLB Pharma, laboratorio que comercializaba el fármaco, y a suspender tanto su actividad como la de Laboratorios Ramallo, empresa que elaboraba productos para HLB sin contar con las autorizaciones necesarias. La causa recayó en el juzgado federal de Ernesto Kreplak y se encuentra en plena etapa de recolección de pruebas.