
La medicina de precisión sumó en las últimas semanas un nuevo avance: la capacidad de detectar fibrosis hepática y cirrosis mediante un simple análisis de sangre basado en inteligencia artificial.
Investigadores del Centro Oncológico Kimmel de Johns Hopkins presentaron en la revista Science Translational Medicine una tecnología capaz de identificar estas enfermedades crónicas en etapas iniciales, mucho antes de que provoquen síntomas irreversibles.
El descubrimiento marca un salto en el uso de las llamadas biopsias líquidas, métodos menos invasivos que la biopsia tradicional y que prometen transformar la atención médica para millones de pacientes.
“Han utilizado un análisis de sangre (ADN fetal libre) para detectar cáncer o anomalías fetales prenatales. Resulta que puede utilizarse para detectar enfermedades hepáticas y mortalidad por cualquier causa debido a otras afecciones”, explicó el médico cardiólogo Eric Topol en la red social X.
Como señaló el médico investigador Eric Topol en declaraciones recogidas por Nature, “Es bueno obtener un resultado negativo en una prueba, pero aún podrías tener cáncer”. El especialista advirtió sobre los riesgos de diagnósticos erróneos y la ansiedad que pueden provocar en los pacientes.
Los nuevos hallazgos
El estudio, dirigido por Victor Velculescu, codirector del programa de genética y epigenética del cáncer en Johns Hopkins, y la doctora Akshaya Annapragada, propone analizar el ADN libre de células (cfDNA) presente en la sangre.
A través de la secuenciación del genoma completo y algoritmos de aprendizaje automático, el equipo logró detectar patrones específicos de fragmentación del ADN asociados a enfermedades hepáticas y otras patologías crónicas.
Según los investigadores, esta tecnología de fragmentación ya se había utilizado en la investigación del cáncer, pero fue la primera vez que se aplicó de manera sistemática a trastornos de origen no oncológico.
“Esto se basa directamente en nuestro trabajo anterior sobre fragmentomas en el cáncer, pero ahora utiliza IA y perfiles de fragmentación de todo el genoma del ADN libre de células para centrarse en las enfermedades crónicas”, explicó Velculescu.
El método no busca mutaciones individuales, sino que evalúa cómo se cortan, empaquetan y distribuyen millones de fragmentos de ADN a lo largo del genoma, un enfoque que permite identificar señales fisiológicas de daño hepático antes de que se manifiesten clínicamente.
La investigación estudió 1.576 individuos con enfermedades hepáticas y otras comorbilidades. El equipo analizó cerca de 40 millones de fragmentos de ADN por paciente, una escala de datos inédita en pruebas de biopsia líquida. A través de modelos de inteligencia artificial, los científicos desarrollaron un sistema de clasificación que detectó enfermedad hepática inicial, fibrosis avanzada y cirrosis con una sensibilidad superior a la de los análisis sanguíneos tradicionales.
“Las biopsias líquidas accesibles, incluyendo análisis de la fragmentación del ADN libre de células (cfDNA) a nivel de genoma, están surgiendo para la detección temprana del cáncer, pero permanecen en gran parte inexploradas en otras enfermedades”, explicó Annapragada, y subrayó el potencial de esta herramienta para identificar alteraciones inmunomediadas y fisiológicas en circulación, no solo en el hígado, sino también en afecciones vasculares, autoinmunes y neurodegenerativas.
El impacto de la detección temprana de la fibrosis hepática no es menor. Según cifras nacionales, en Estados Unidos alrededor de 100 millones de personas presentan afecciones hepáticas que incrementan el riesgo de cirrosis y cáncer. La fibrosis, en etapas iniciales, resulta reversible, pero una vez que progresa a cirrosis, el daño puede ser permanente y aumentar considerablemente el riesgo de cáncer de hígado.
Las técnicas actuales, como las imágenes por ultrasonido o resonancia magnética, requieren tecnología especializada y, en muchos casos, no logran identificar la enfermedad en fases tempranas. Los análisis sanguíneos tradicionales solo detectan cirrosis en aproximadamente la mitad de los casos y muestran baja eficacia para la fibrosis incipiente.
“Muchas personas en riesgo desconocen que padecen una enfermedad hepática. Si podemos intervenir antes, antes de que la fibrosis progrese a cirrosis o cáncer, el impacto podría ser considerable”, sostuvo Velculescu. Los investigadores plantean que la detección precoz no solo alerta sobre la presencia de daño hepático, sino que también puede identificar condiciones tratables y prevenir la evolución hacia el cáncer.
El funcionamiento de la biopsia líquida y el fragmentoma

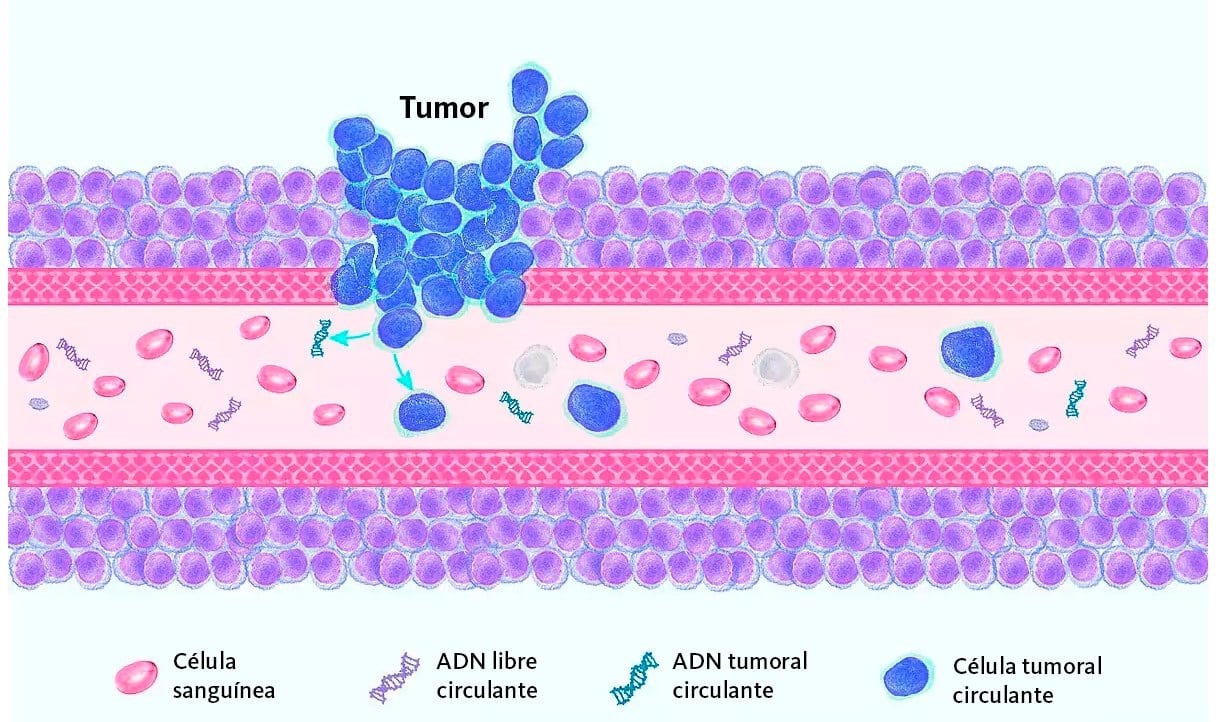
La biopsia líquida consiste en la obtención de información biológica a partir de fluidos corporales, principalmente sangre.
En oncología, esta técnica ya se utiliza para localizar células tumorales circulantes (CTC), ADN tumoral y vesículas extracelulares.
El nuevo enfoque desarrollado por el equipo de Johns Hopkins se centra en el análisis del fragmentoma, el conjunto de fragmentos de ADN libre de células que se liberan cuando las células mueren y se degradan.
Esta información puede revelar no solo la presencia de tumores, sino también lesiones y procesos inflamatorios en órganos como el hígado.
La clave está en la aplicación de inteligencia artificial a la secuenciación masiva del genoma. El sistema analiza la longitud, la ubicación y los patrones de los fragmentos de ADN, identificando señales características de fibrosis y cirrosis. Este procedimiento permite desarrollar clasificadores específicos para cada enfermedad, sin riesgo de reacción cruzada entre diferentes patologías.
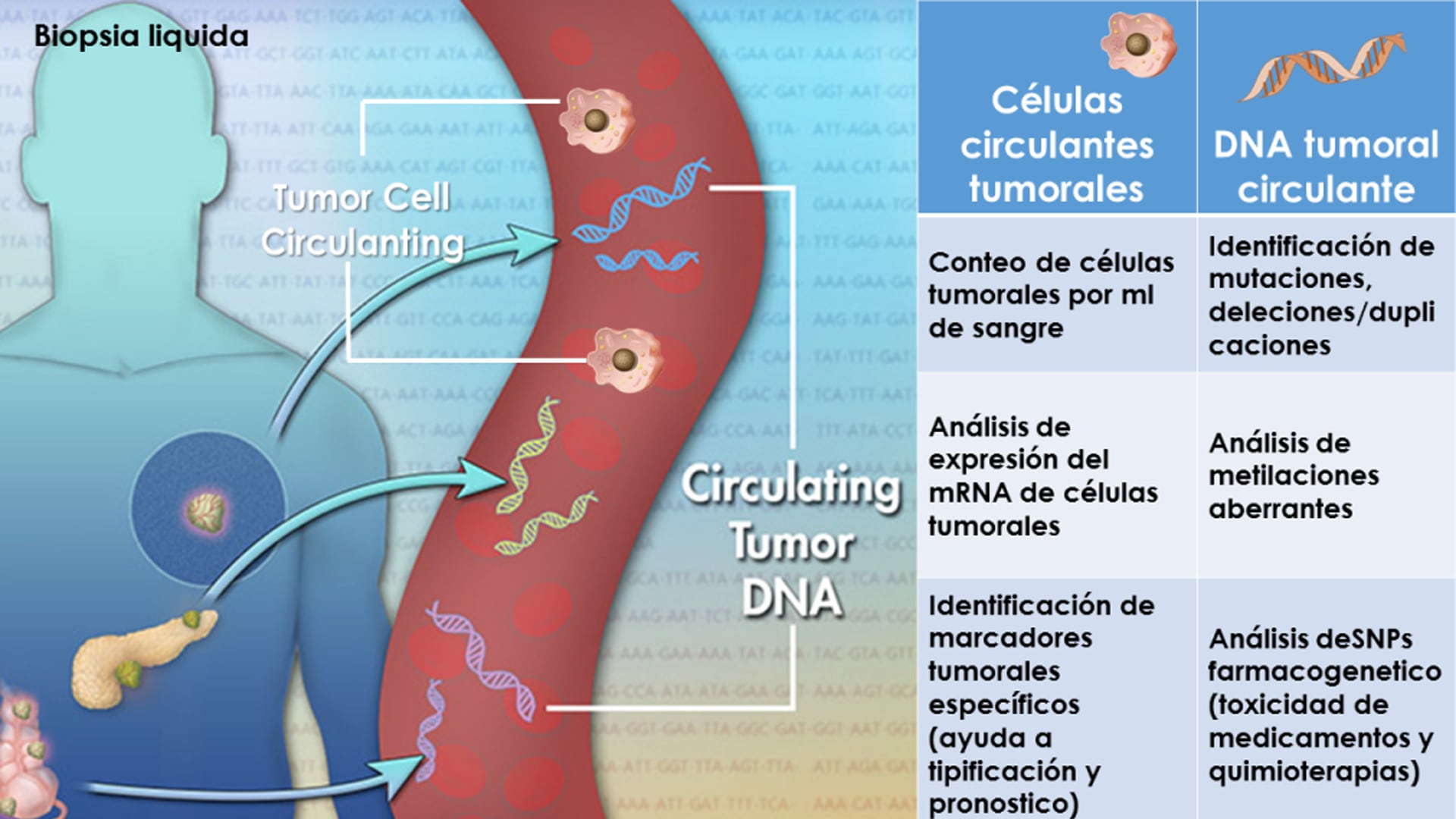
Así lo explicó Annapragada: “El fragmentoma puede servir de base para crear diferentes clasificadores para distintas enfermedades y, lo que es más importante, estos clasificadores son específicos de cada enfermedad y no presentan reacciones cruzadas. Un clasificador de fibrosis hepática es distinto de un clasificador de cáncer. Esta es una prueba única y específica para cada enfermedad, desarrollada a partir de la misma plataforma subyacente”.
El estudio también avanzó sobre las posibilidades de la biopsia líquida para predecir la supervivencia global de los pacientes. El modelo de aprendizaje automático, entrenado con los datos de fragmentomas, fue capaz de anticipar el pronóstico en diferentes cohortes humanas, superando en algunos casos la especificidad de los marcadores inflamatorios clásicos y el índice de comorbilidad de Charlson.
Un salto frente a los análisis tradicionales
El auge de los análisis de sangre para la detección de cáncer y otras enfermedades crónicas ha generado debate en la comunidad científica. Pruebas como Galleri, desarrollada por GRAIL, o CancerSEEK y Cancerguard apuntan a diagnosticar múltiples tipos de cáncer en etapas tempranas a partir de marcadores en sangre. Sin embargo, según reportó Nature en un extenso artículo, la mayoría de estas pruebas no ha superado aún ensayos clínicos aleatorizados, considerados el estándar de oro para su validación. Ninguna recibió todavía aprobación regulatoria definitiva.
Los análisis multicáncer de sangre muestran alta especificidad —identifican correctamente la ausencia de cáncer en hasta el 99,5 % de los casos—, pero su sensibilidad varía según el tipo y estadio del cáncer.
La tecnología del fragmentoma, en cambio, propone un abordaje diferente. No se limita a rastrear mutaciones específicas, sino que explora la arquitectura global del ADN circulante, lo cual extiende su utilidad a enfermedades crónicas no cancerosas.
El estudio de Johns Hopkins incluyó análisis de fragmentomas y metilomas, identificando no solo alteraciones hepáticas, sino también cambios inmunomediados en patologías vasculares y neurodegenerativas.
Un aspecto destacado por los autores fue la capacidad del método para anticipar el pronóstico de los pacientes. “Un modelo de aprendizaje automático que utiliza fragmentomas de cfDNA predijo la supervivencia global en cohortes separadas de descubrimiento de morbilidad y validación”, precisó Annapragada en la publicación.

El desarrollo de esta tecnología abre la puerta a métodos de diagnóstico y seguimiento menos invasivos, capaces de monitorear el estado fisiológico de los pacientes en tiempo real y ajustar los tratamientos de manera personalizada.
Según los expertos, la posibilidad de realizar muestreos repetidos sin recurrir a biopsias invasivas representa una ventaja tanto para la medicina de precisión como para la experiencia del paciente.
Los desafíos futuros incluyen la validación en ensayos clínicos más amplios y la integración de estas herramientas en la práctica médica cotidiana. Mientras tanto, la promesa de detectar enfermedades hepáticas y otras patologías crónicas con una simple muestra de sangre ya transformó el horizonte de la prevención y el tratamiento personalizado.
