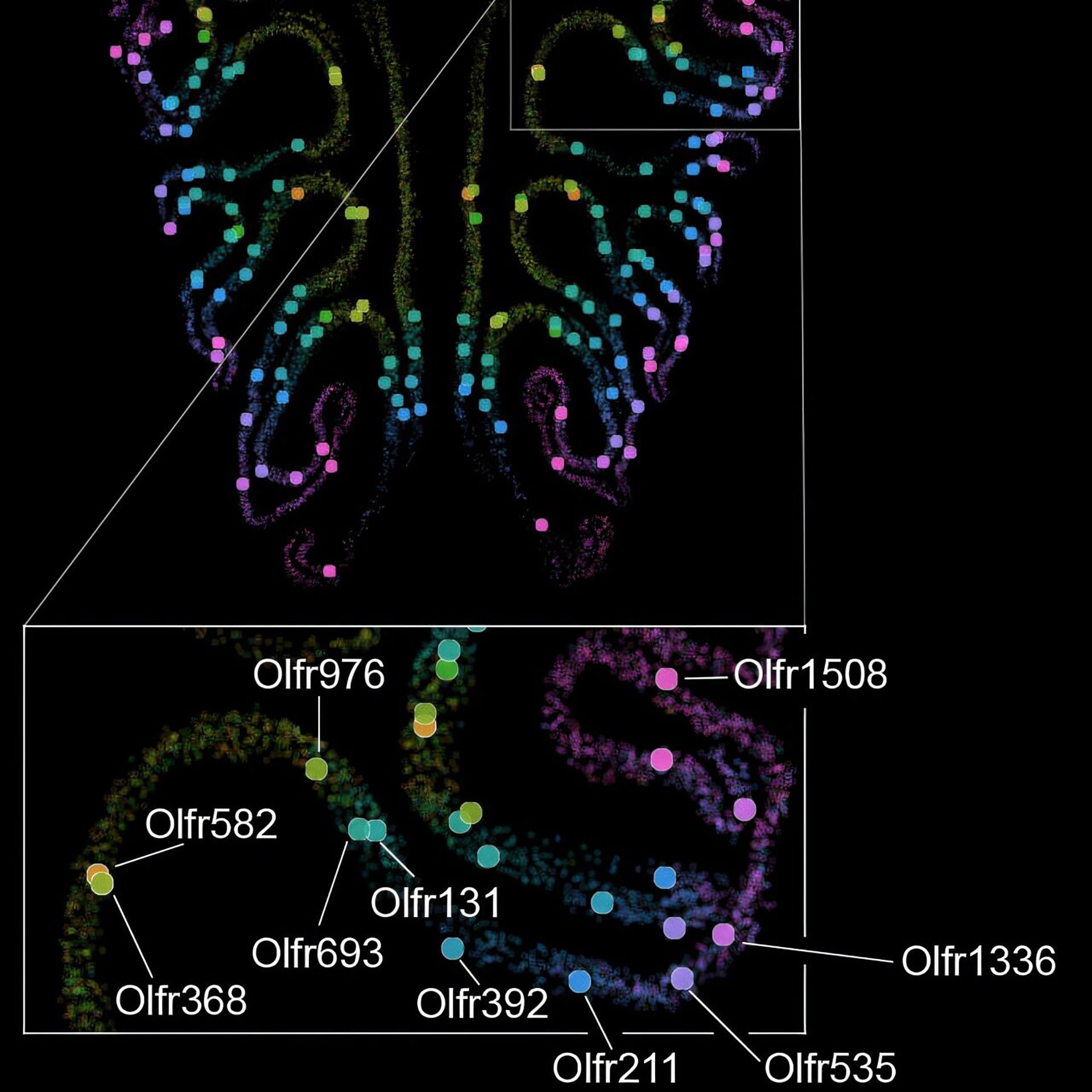
Un equipo liderado por Sandeep Robert Datta, profesor de neurobiología en el Instituto Blavatnik de la Facultad de Medicina de Harvard, ha modificado de raíz la visión sobre el sentido del olfato al revelar el primer mapa detallado de la organización espacial de los más de mil tipos de receptores olfativos presentes en la nariz de los mamíferos. Tras analizar más de 5,5 millones de neuronas en 300 ratones, los investigadores demostraron que, lejos de la aleatoriedad que suponía la biología desde hace tres décadas, las neuronas olfativas siguen un patrón estructurado: se distribuyen en franjas horizontales superpuestas en función del receptor que expresan, desde la parte superior hasta la inferior de la nariz.
Los científicos descubrieron que la posición de cada receptor depende de un gradiente de ácido retinoico y de la activación coordinada de cientos de genes reguladores, lo que permite que las neuronas olfativas se organicen en franjas precisas y que este patrón se repita en todos los individuos.
Este hallazgo resulta interesante porque rompe con 35 años de creencias sobre el olfato y acerca su comprensión a la de otros sentidos como la visión o el oído. Además, abre la puerta al desarrollo de nuevas terapias para la pérdida del olfato, un problema sin soluciones eficaces y con impacto profundo en la salud y el bienestar.
Los resultados, publicados en la revista Cell, corregirán la interpretación de libros de texto y abren la puerta a explicar por qué la pérdida del olfato por enfermedades o lesiones sigue siendo tan poco conocida y tiene tratamientos insuficientes. Datta subrayó que “el olfato es sumamente misterioso y nuestra comprensión biológica básica está por detrás de la visión, el oído y el tacto”, y enfatizó que su trabajo “aporta orden a un sistema que antes se consideraba carente de él, lo que cambia conceptualmente nuestra forma de pensar sobre su funcionamiento”.
Un hallazgo complementario del estudio es la coincidencia del mapa de receptores en la nariz con los mapas olfativos en el bulbo olfatorio del cerebro, lo que implica una continuidad topográfica desde la percepción molecular en la epitelio nasal hasta el procesamiento cerebral. El equipo validó esta correspondencia tras observar que las posiciones espaciales de los receptores en la nariz predecían con exactitud la localización tridimensional de los glomérulos a los que proyectan las neuronas. En palabras de Datta: “Demostramos que el desarrollo puede lograr esta hazaña de organizar mil receptores olfativos diferentes en un mapa increíblemente preciso que es consistente en todos los animales”.
El ácido retinoico define el mapa olfativo con precisión celular
Los investigadores identificaron el ácido retinoico como factor determinante de la organización: un gradiente de esta molécula a lo largo de la nariz condiciona a cada neurona en la elección de su receptor, asegurando así que el patrón se replique en todos los individuos y que cualquier alteración en este gradiente derive en un desplazamiento del mapa de receptores. Añadir o eliminar ácido retinoico desplazó las posiciones de los receptores hacia arriba o abajo en el epitelio nasal.
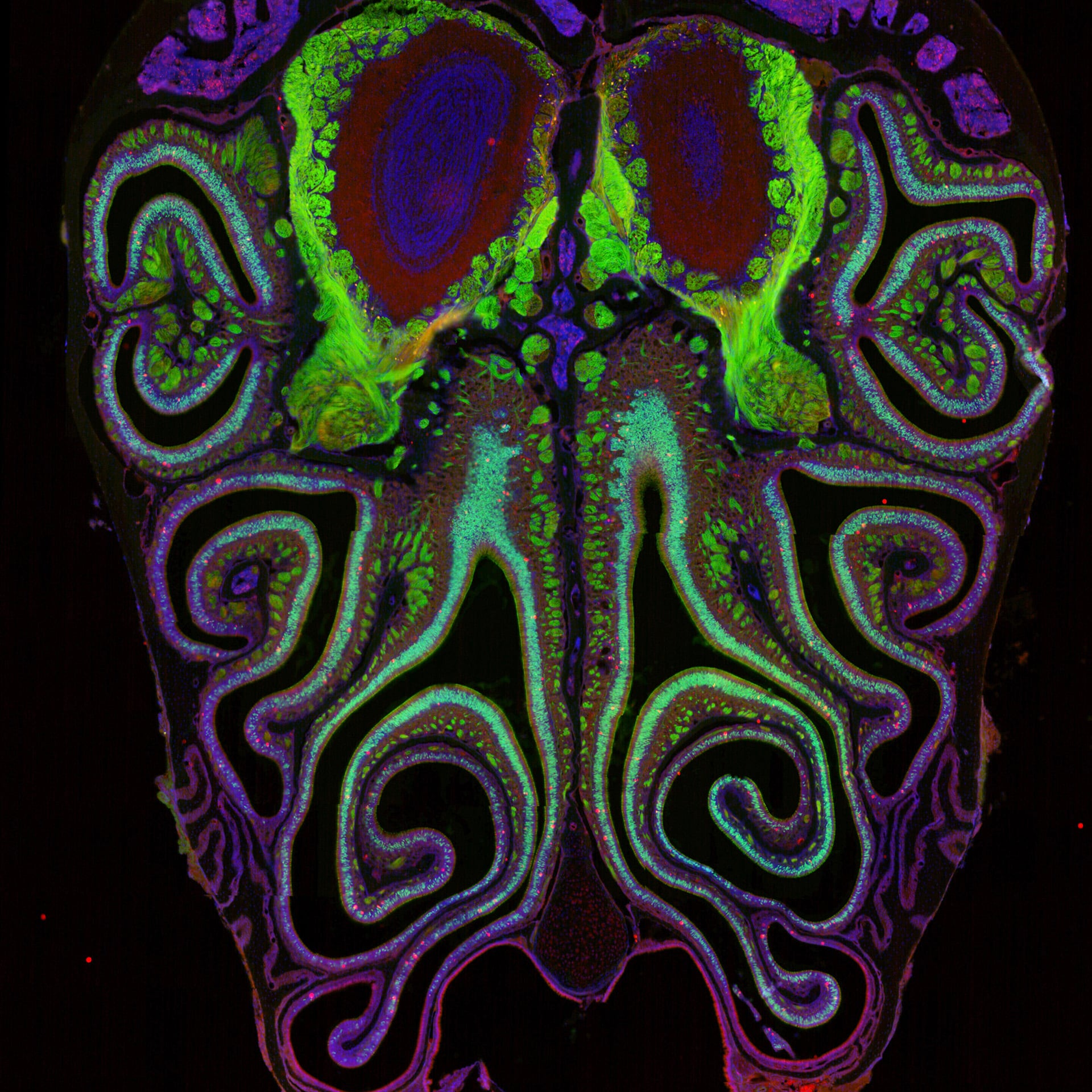
En paralelo, los experimentos de manipulación genética demostraron que la identidad espacial de las neuronas precursoras ya codifica información relacionada con su ubicación antes de la expresión del receptor específico. Esta identidad espacial, medida mediante la expresión coordinada de cerca de 250 genes, anticipa el tipo de receptor olfativo que la neurona terminará expresando y, por tanto, expresa un orden biológico profundo, contrario a la hipótesis dominante de aleatoriedad dentro de “zonas” amplias.

Las técnicas empleadas incluyeron la secuenciación de células individuales y análisis transcriptómico espacial, lo que convierte a este tejido en el área neuronal más minuciosamente cartografiada hasta la fecha. “Podría decirse que este es el tejido neuronal más secuenciado de la historia, pero necesitábamos esa cantidad de datos para comprender el sistema”, sostuvo uno de los investigadores.
Fractura de un paradigma: del azar al patrón genómico regulado

Durante 35 años, la biología consideró que, a diferencia de los sentidos visual, auditivo y táctil, el olfato carecía de un mapa definido. Lo sustentaba el hecho de que los ratones—con más de 1.100 tipos de receptores olfativos y unos 20 millones de neuronas dedicadas a este sentido—muestran una expresión molecular que, hasta ahora, parecía agruparse en zonas laxas dentro del tejido.
Sin embargo, los resultados de Harvard revelan que cada tipo de la enorme familia de receptores ocupa una posición promedio única y predecible a lo largo del eje dorsoventral, lo que confiere al epitelio olfativo un grado de organización anatómica semejante al de otros sistemas sensoriales.
La clave reside en la coordinación de programas genéticos compuestos por centenares de genes reguladores, entre los que predominan factores de transcripción, como la familia NFI, responsables del silenciamiento selectivo mediante heterocromatina de los genes de receptores que no corresponden a la posición espacial de cada célula. Este mecanismo asegura que sólo los receptores apropiados sean activados en las posiciones correctas del epitelio, estabilizando así el mapa a lo largo del tiempo y las generaciones.
Una de las pruebas críticas fue la observación de que la manipulación del gradiente de ácido retinoico o de los componentes del sistema de silenciamiento génico provoca desplazamientos coherentes en el patrón de expresión de los receptores. Además, el análisis de híbridos entre distintas cepas de ratón permitió verificar que cambios en regiones no codificantes del ADN explican las variaciones en la posición espacial de los receptores entre linajes, sin modificar la secuencia funcional de las proteínas.
“Ahora podemos explicar por qué las neuronas vecinas eligen receptores similares y proyectan al mismo lugar en el cerebro”, detallaron los investigadores.
Del mapa básico al impacto en la salud y la tecnología
Robert Sandeep remarcó un horizonte concreto: “No podemos solucionar el problema del olfato sin comprender cómo funciona a nivel básico”, expuso. Hoy, la falta de terapias eficaces para la pérdida del olfato, agudizada por fenómenos como la COVID-19, representa una frontera científica no resuelta. El nuevo mapa plantea el diseño de estrategias como terapias con células madre, edición génica o el desarrollo de interfaces cerebro-computadora que restaure la función sensorial precisando exactamente qué receptores y neuronas reconstruir.
El grupo extiende los experimentos a tejido humano para determinar si el patrón descrito en ratones se reproduce en nuestra especie. Según Datta: “El olfato tiene un efecto profundo y generalizado en la salud humana, por lo que recuperarlo no sólo aporta placer y seguridad, sino también bienestar psicológico. Sin comprender este mecanismo, estamos condenados al fracaso en el desarrollo de nuevos tratamientos”.
Los hallazgos modifican la concepción misma de la biología sensorial e instalan un nuevo principio: la organización espacial es universal en todos los sentidos y responde a regulaciones moleculares que trascienden la percepción para influir en salud mental y calidad de vida.