Detectar enfermedades antes de que aparezcan los síntomas puede cambiar por completo el curso de la vida. Bajo esa premisa, el Reino Unido avanza con un ambicioso programa de cribado genético neonatal, una estrategia que busca identificar trastornos poco frecuentes en los primeros días de vida y actuar antes de que causen daño.
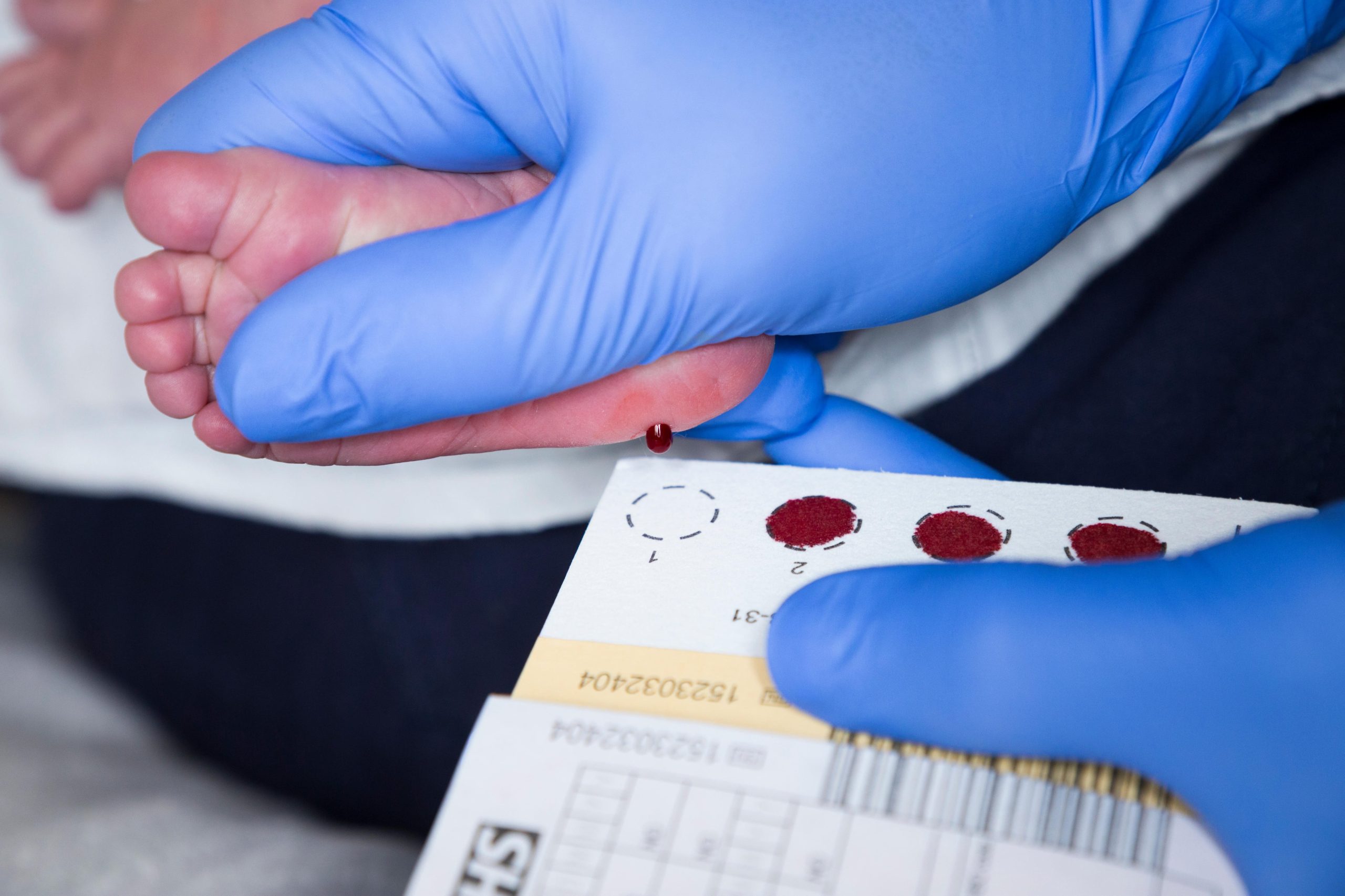
El cribado neonatal —también conocido como “test del talón”— es un conjunto de pruebas que se realizan a los recién nacidos a partir de una pequeña muestra de sangre. Su objetivo es detectar enfermedades graves que no presentan signos visibles al nacer, pero que pueden afectar el desarrollo si no se tratan a tiempo.
En este contexto, Escocia dio un paso decisivo al incorporar la detección de atrofia muscular espinal en este test, mientras que en Inglaterra se desarrolla el Generation Study, anunciado en 2023 y puesto en marcha progresivamente desde 2024, un proyecto que amplía el alcance del diagnóstico mediante el análisis del ADN completo de los bebés.
En conjunto, estas iniciativas posicionan al país como referente en prevención médica infantil basada en herramientas genéticas.

A diferencia del cribado tradicional —que detecta un número limitado de patologías—, la secuenciación genómica permite identificar más de 200 enfermedades raras desde el nacimiento, muchas de ellas tratables si se detectan a tiempo, según datos del NHS (Servicio Nacional de Salud del Reino Unido).
La experiencia piloto en Escocia
Escocia se convirtió en la primera región del Reino Unido en ofrecer detección universal de la atrofia muscular espinal (SMA, por sus siglas en inglés) dentro del cribado neonatal. La prueba se realiza con la misma muestra de sangre obtenida a los pocos días de vida, sin necesidad de procedimientos adicionales, de acuerdo con The Guardian.
Esta enfermedad genética afecta aproximadamente a 1 de cada 14.000 recién nacidos y provoca una degeneración progresiva de las neuronas motoras, responsables de controlar el movimiento. Sin tratamiento, puede reducir la expectativa de vida a menos de dos años, según el medio británico.

El diagnóstico temprano es fundamental, ya que el daño neurológico no puede revertirse una vez que aparecen los síntomas. Actualmente, el sistema de salud británico dispone de terapias capaces de modificar el curso de la enfermedad, pero su eficacia depende de una detección precoz.
Desde organizaciones especializadas destacan que este avance marca un cambio significativo respecto a años anteriores, cuando el diagnóstico se realizaba en etapas más avanzadas. Además, el hecho de que 1 de cada 40 adultos sea portador del gen alterado evidencia la importancia de identificar estos casos de forma temprana, según datos recopilados por The Guardian.
Generation Study: anticipar enfermedades desde el ADN
En paralelo, el Generation Study representa el mayor programa de secuenciación genómica neonatal en Europa. Su objetivo es analizar el genoma completo de 100.000 recién nacidos en hospitales de Inglaterra para detectar enfermedades raras tratables antes de que se manifiesten, según el Newborn Genomes Programme.
El genoma es el conjunto completo de información genética de una persona. Analizarlo permite identificar alteraciones asociadas a distintas enfermedades, incluso antes de que generen síntomas. A diferencia de los métodos tradicionales, esta tecnología amplía de forma considerable la capacidad de diagnóstico.

La muestra se obtiene del cordón umbilical y la participación es voluntaria, independiente del cribado estándar. La iniciativa busca incluir familias de distintos contextos sociales y culturales, promoviendo un acceso equitativo a esta innovación.
Los datos se almacenan bajo estrictas condiciones de seguridad en la National Genomic Research Library, donde solo investigadores autorizados pueden acceder a información anonimizada, de acuerdo con el Newborn Genomes Programme.
Beneficios clínicos y desafíos éticos
El principal beneficio de estas estrategias es la posibilidad de intervenir en etapas tempranas, cuando los tratamientos pueden ser más efectivos. En muchos casos, iniciar una terapia en los primeros meses de vida puede evitar complicaciones graves o mejorar de forma sustancial el desarrollo.
Un ejemplo es el caso de Safi Ford, diagnosticada precozmente con una deficiencia hormonal gracias al Generation Study. El tratamiento iniciado en los primeros meses permitió una evolución favorable en poco tiempo, según información difundida por el NHS.

Sin embargo, estos avances también plantean desafíos. El manejo de información genética requiere consentimiento informado, protección de datos y criterios claros sobre qué resultados comunicar a las familias.
Además, existe el riesgo de que estas tecnologías generen desigualdades si no se garantiza su acceso en todos los sectores de la población. Por este motivo, el diseño del programa incluyó la participación de especialistas, pacientes y comunidades diversas, con el objetivo de abordar estas cuestiones desde una perspectiva ética, según el Newborn Genomes Programme.
Un cambio en la forma de entender la salud
El impulso del cribado genético neonatal en el Reino Unido refleja un cambio profundo en la medicina: pasar de tratar enfermedades a anticiparlas.
Cada año, miles de niños nacen con condiciones genéticas cuyo diagnóstico tardío limita las opciones de tratamiento cuando la enfermedad ya está avanzada. La posibilidad de identificar estos casos desde los primeros días de vida no solo mejora las oportunidades terapéuticas, sino que redefine el enfoque del sistema de salud.
A medida que estas tecnologías avanzan, el desafío será equilibrar sus beneficios con una implementación responsable. En ese escenario, el cribado genético no solo representa una herramienta diagnóstica, sino también una nueva forma de pensar la salud desde el inicio de la vida.